Ste vedeli? Proces odkrivanja ljudiyttriumje bil poln zasukov in izzivov. Leta 1787 je švedski Karl Axel Arrhenius po nesreči odkril gosto in težko črno rudo v kamnolomu v bližini domačega kraja Ytterby Village in jo poimenoval "ytterbite". Po tem so številni znanstveniki, vključno z Johanom Gadolinom, Andersom Gustavom Ekbergom, Friedrichom Wöhlerjem in drugimi, poglobljeno raziskali to rudo.
Leta 1794 je finski kemik Johan Gadolin uspešno ločil nov oksid od ytterbium rude in ga poimenoval yttrium. To je bilo prvič, da so ljudje jasno odkrili redek zemeljski element. Vendar to odkritje ni takoj pritegnilo široke pozornosti.
Sčasoma so znanstveniki odkrili druge redke zemeljske elemente. Leta 1803 sta nemška Klaproth in Švedi Hitzinger in Berzelius odkrila Cerium. Leta 1839 je odkril švedski MosanderLanthanum. Leta 1843 je odkril Erbium interbij. Ta odkritja so postala pomemben temelj za poznejše znanstvene raziskave.
Šele konec 19. stoletja so znanstveniki uspešno ločili element "yttrium" iz yttrium rude. Leta 1885 je avstrijski Wilsbach odkril neodimij in praseodim. Leta 1886 je odkril Bois-Baudrandisprozija. Ta odkritja so še bolj obogatila veliko družino redkih zemeljskih elementov.
Znanstveniki zaradi omejitev tehničnih razmer že več kot stoletja po odkritju Ytrija niso mogli očistiti tega elementa, kar je povzročilo tudi nekatere akademske spore in napake. Vendar to znanstvenikom ni preprečilo njihovega navdušenja nad študijem Yttrium.
V začetku 20. stoletja so znanstveniki z nenehnim napredkom znanosti in tehnologije končno začeli čistiti redke zemeljske elemente. Leta 1901 je odkril Francoz Eugene de Marseilleeuropium. V letih 1907-1908 sta avstrijski Wilsbach in Francoz Urbain neodvisno odkrila lutecij. Ta odkritja so postala pomemben temelj za poznejše znanstvene raziskave.
V sodobni znanosti in tehnologiji je uporaba Yttrium vse bolj obsežna. Z nenehnim napredkom znanosti in tehnologije bo naše razumevanje in uporaba yttrija vedno bolj poglobljena.
Aplikacijska polja elementa yttrium
1.Optično steklo in keramika:Yttrium se pogosto uporablja pri proizvodnji optičnega stekla in keramike, predvsem pri izdelavi prozorne keramike in optičnega stekla. Njegove spojine imajo odlične optične lastnosti in jih je mogoče uporabiti za izdelavo komponent laserjev, optičnih komunikacij in druge opreme.
2. Fosfor:Yttrium spojine igrajo pomembno vlogo pri fosforjih in lahko oddajajo svetlo fluorescenco, zato se pogosto uporabljajo za izdelavo televizijskih zaslonov, monitorjev in osvetlitvene opreme.Yttrium oksidin druge spojine se pogosto uporabljajo kot svetilke za izboljšanje svetlosti in jasnosti svetlobe.
3. Additivi zlitine: Pri proizvodnji kovinskih zlitin se Ytrium pogosto uporablja kot dodatek za izboljšanje mehanskih lastnosti in korozijske odpornosti kovin.Zlitine yttriumse pogosto uporabljajo za izdelavo jekla z visoko trdnostjo inAluminijeve zlitine, zaradi česar so bolj odporni na toploto in odporne proti koroziji.
4. katalizatorji: Spojine Yttrium igrajo pomembno vlogo pri nekaterih katalizatorjih in lahko pospešijo hitrost kemičnih reakcij. Uporabljajo se za proizvodnjo avtomobilskih naprav za čiščenje izpušnih plinov in katalizatorjev v industrijskih proizvodnih procesih, kar pomaga zmanjšati emisije škodljivih snovi.
5. Medicinska tehnologija slikanja: Izotopi Yttrium se uporabljajo v tehnologiji medicinske slikanje za pripravo radioaktivnih izotopov, na primer za označevanje radiofarmacevtskih izdelkov in diagnosticiranje jedrskega medicinskega slikanja.
6. laserska tehnologija:Yttrium ionski laserji so pogost laser v trdnem stanju, ki se uporablja v različnih znanstvenih raziskavah, laserskih medicini in industrijskih aplikacijah. Proizvodnja teh laserjev zahteva uporabo nekaterih spojin Ytrium kot aktivatorjev.Yttrium elementiIn njihove spojine igrajo pomembno vlogo v sodobni znanosti in tehnologiji in industriji, ki vključujejo številna področja, kot so optika, znanost o materialih in medicina, in pozitivno prispevali k napredku in razvoju človeške družbe.
Fizikalne lastnosti yttrium
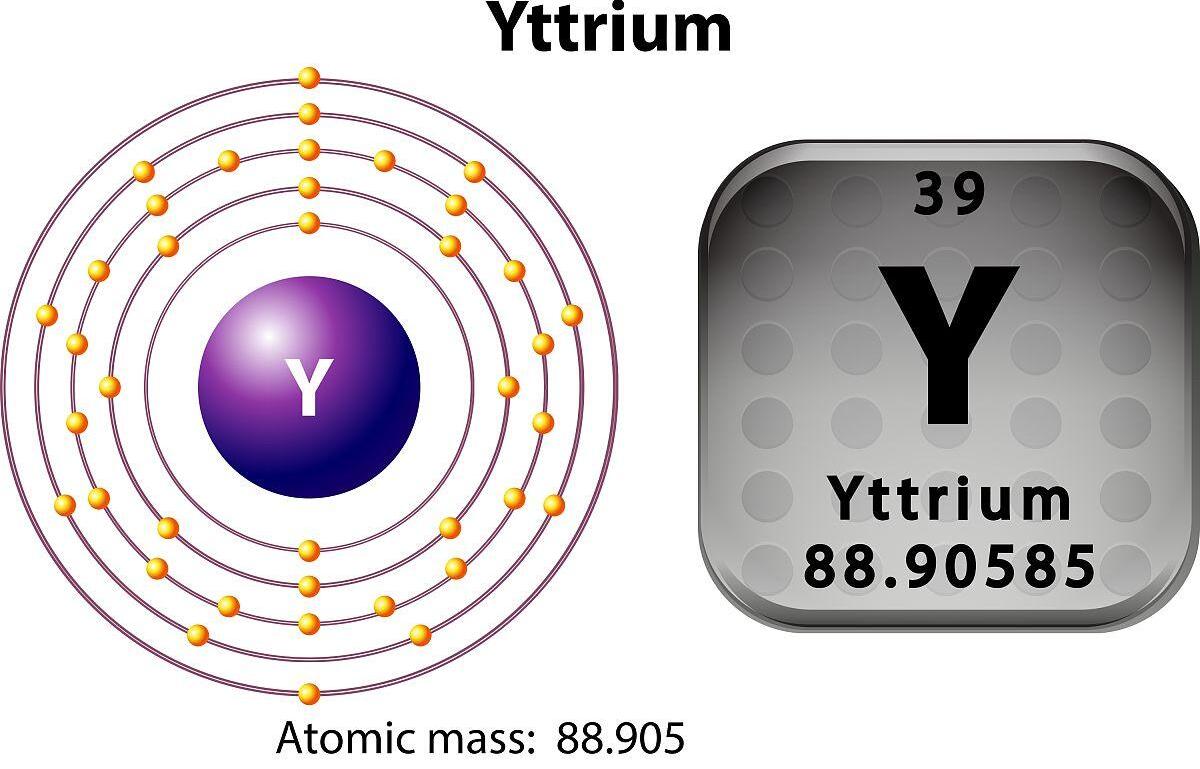
Atomsko številoyttriumje 39, njegov kemični simbol pa je Y.
1. videz:Yttrium je srebrno bela kovina.
2. Gostota:Gostota ytrija je 4,47 g/cm3, zaradi česar je eden izmed relativno težkih elementov v Zemljini skorji.
3. Tališče:Tališče Yttrium je 1522 stopinj Celzija (2782 stopinj Fahrenheita), ki se nanaša na temperaturo, pri kateri se ytrium v toplotnih pogojih spremeni iz trdne v tekočino.
4. vrelišče:Točka vrelišča Yttrium je 3336 stopinj Celzija (6037 stopinj Fahrenheita), ki se nanaša na temperaturo, pri kateri se Ytrium v toplotnih pogojih spreminja iz tekočine v plin.
5. faza:Pri sobni temperaturi je yttrium v trdnem stanju.
6. Prevodnost:Yttrium je dober prevodnik električne energije z visoko prevodnostjo, zato ima določene aplikacije v tehnologiji proizvodnje in vezja elektronskih naprav.
7. magnetizem:Yttrium je paramagnetni material pri sobni temperaturi, kar pomeni, da nima očitnega magnetnega odziva na magnetna polja.
8. kristalna struktura: Yttrium obstaja v šesterokotni tesno pakirani kristalni strukturi.
9. Atomski volumen:Atomski volumen Yttrium je 19,8 kubičnih centimetrov na mol, kar se nanaša na prostornino, ki ga zaseda en krti atomov yttrijeve.
Yttrium je kovinski element z relativno visoko gostoto in tališčem in ima dobro prevodnost, zato ima pomembne aplikacije na področju elektronike, materialov in drugih področjih. Hkrati je Ytrium tudi razmeroma pogost redek element, ki ima pomembno vlogo pri nekaterih naprednih tehnologijah in industrijskih aplikacijah.
Kemične lastnosti yttrium
1. Kemični simbol in skupina: Kemični simbol ytrija je y in se nahaja v petem obdobju periodične tabele, tretje skupine, ki je podobna elementom lantanida.
2. Elektronska struktura: Elektronska struktura Yttrium je 1S² 2s² 2p⁶ 3S² 3p⁶ 3d¹⁰ 4S² 4p⁶ 4d¹⁰ 4f¹⁴ 5S². V zunanji plasti elektronov ima yttrium dva valenčna elektrona.
3. Stanje Valence: Yttrium običajno prikazuje valenčno stanje +3, kar je najpogostejše valenčno stanje, lahko pa kaže tudi valenčna stanja +2 in +1.
4. Reaktivnost: ytrium je razmeroma stabilna kovina, vendar bo postopoma oksidirala, ko bo izpostavljena zraku, na površini tvori oksidno plast. To povzroči, da yttrium izgubi sijaj. Za zaščito Yttrium ga običajno shranimo v suhem okolju.
5. Reakcija z oksidi: ytrium reagira z oksidi, da tvori različne spojine, vključno zyttrium oksid(Y2O3). Yttrium oksid se pogosto uporablja za izdelavo fosfor in keramike.
6. ** Reakcija s kislinami **: ytrium lahko reagira z močnimi kislinami, da ustvari ustrezne soli, kot soYttrium klorid (Ycl3) aliyttrium sulfat (Y2 (SO4) 3).
7. Reakcija z vodo: yttrium ne reagira neposredno z vodo v normalnih pogojih, pri visokih temperaturah pa lahko reagira z vodno paro, da nastane vodik in ytrijev oksid.
8. Reakcija s sulfidi in karbidi: yttrium lahko reagira s sulfidi in karbidi, da tvori ustrezne spojine, kot sta yttrium sulfid (ys) in ytrium karbid (yc2). 9. Izotopi: Yttrium ima več izotopov, od katerih je najbolj stabilen Ytrium-89 (^89y), ki ima dolgo razpolovno dobo in se uporablja pri označevanju jedrske medicine in izotopov.
Yttrium je razmeroma stabilen kovinski element z več valenčnimi stanji in sposobnost reagiranja z drugimi elementi, da tvori spojine. Ima široko paleto aplikacij za optiko, znanost o materialih, medicino in industrijo, zlasti v fosforjih, proizvodnji keramike in laserske tehnologije.
Biološke lastnosti yttrium
Biološke lastnostiyttriumV živih organizmi so razmeroma omejeni.
1. Prisotnost in zaužitje: Čeprav yttrium ni element, ki je bistven za življenje, je v naravi mogoče najti količine yttrija v sledovih, vključno z zemljo, skalami in vodo. Organizmi lahko zaužijejo sledi Ytrium skozi prehransko verigo, običajno iz zemlje in rastlin.
2. Biološka uporabnost: Biološka uporabnost Yttrium je razmeroma nizka, kar pomeni, da imajo organizmi na splošno težave pri absorpciji in uporabi yttrium. Večina ytrium spojin ni enostavno absorbirati v organizmih, zato se ponavadi izločajo.
3. Porazdelitev v organizmih: Ko v organizmu, se ytrium porazdeli predvsem v tkivih, kot so jetra, ledvice, vranica, pljuča in kosti. Zlasti kosti vsebujejo večje koncentracije yttrium.
4. Metabolizem in izločanje: Presnova ytrija v človeškem telesu je razmeroma omejena, ker običajno zapusti organizem z izločanjem. Večina se izloča skozi urin, prav tako pa se lahko izloči v obliki defekacije.
5. Toksičnost: Ytrium zaradi nizke biološke uporabnosti se v normalnih organizmih običajno ne kopiči na škodljivi ravni. Vendar ima lahko izpostavljenost Ytrium z visokimi odmerki škodljive učinke na organizme, kar vodi do strupenih učinkov. Takšno stanje se ponavadi pojavlja redko, ker so koncentracije ytrija v naravi običajno nizke in se ne uporabljajo pogosto ali izpostavljene organizmom. Biološke značilnosti yttrija v organizmih se kažejo predvsem v njegovi prisotnosti v sledovih, nizki biološki uporabnosti in niso element, ki je potreben za življenje. Čeprav v normalnih okoliščinah nima očitnih strupenih učinkov na organizme, lahko izpostavljenost Ytriumu z visokimi odmerki povzroči nevarnosti za zdravje. Zato so znanstvene raziskave in spremljanje še vedno pomembne za varnosti in biološke učinke yttrija.
Porazdelitev yttrium v naravi
Yttrium je redek zemeljski element, ki je v naravi razmeroma široko razporejen, čeprav ne obstaja v čisti elementarni obliki.
1. Pojav v zemeljski skorji: Številka ytrija v zemeljski skorji je relativno nizka, povprečna koncentracija približno 33 mg/kg. Zaradi tega je Ytrium eden redkih elementov.
Yttrium v glavnem obstaja v obliki mineralov, običajno skupaj z drugimi redkimi zemeljskimi elementi. Nekateri glavni yttrium minerali vključujejo ytrium železni garn (yig) in yttrium oksalat (y2 (c2o4) 3).
2. Geografska porazdelitev: nahajališča Yttrium se porazdelijo po vsem svetu, vendar so nekatera območja morda bogata z ytrijem. Nekatera večja nahajališča Yttrium najdemo v naslednjih regijah: Avstralija, Kitajska, ZDA, Rusija, Kanada, Indija, Skandinavija itd. 3. Ekstrakcija in obdelava: Ko je ruda Yttrium minirana, je za pridobivanje in ločitev Yttrium običajno potrebna kemična obdelava. To običajno vključuje postopke izpiranja kislin in kemičnih ločevanja, da se pridobi z visoko čistostjo yttrium.
Pomembno je opozoriti, da redki zemeljski elementi, kot je ytrium, običajno ne obstajajo v obliki čistih elementov, ampak so mešani z drugimi redkimi zemeljskimi elementi. Zato ekstrakcija večje čistosti yttrium zahteva zapletene kemične procese in ločevanje. Poleg tega dobavaRedki zemeljski elementije omejena, zato je pomembno upoštevanje njihovega upravljanja virov in okoljske trajnosti.
Rudarjenje, ekstrakcija in taljenje elementa yttrium
Yttrium je redek zemeljski element, ki običajno ne obstaja v obliki čistega ytrija, ampak v obliki ytrium rude. Sledi podroben uvod v proces rudarjenja in rafiniranja elementa yttrium:
1. rudarjenje yttrium rude:
Raziskovanje: Prvič, geologi in rudarski inženirji izvajajo raziskovalna dela, da bi našli nahajališča, ki vsebujejo yttrium. To običajno vključuje geološke študije, geofizično raziskovanje in analizo vzorcev. Rudarstvo: Ko najdemo nahajališče, ki vsebuje yttrium, se ruda minira. Te nahajališča običajno vključujejo oksidne rude, kot sta železov granat Yttrium (YIG) ali ytrium oksalat (Y2 (C2O4) 3). Ruda drobljenje: po rudarjenju je treba rudo običajno razbiti na manjše koščke za nadaljnjo obdelavo.
2. Ekstrahiranje yttrium:Kemično izpiranje: zdrobljena ruda se običajno pošlje v talilnico, kjer se yttrium pridobiva s kemičnim izpiranjem. Ta postopek običajno uporablja kislo raztopino izpiranja, kot je žveplova kislina, za raztapljanje ytrija iz rude. Ločitev: Ko se yttrium raztopi, ga običajno mešamo z drugimi redkimi zemeljskimi elementi in nečistočami. Za ekstrahiranje ytrija večje čistosti je potreben postopek ločevanja, običajno z uporabo ekstrakcije topila, ionske izmenjave ali drugih kemičnih metod. Padavine: Yttrium se loči od drugih redkih zemeljskih elementov z ustreznimi kemičnimi reakcijami, da tvorijo čiste ytrium spojine. Sušenje in kalcinacija: dobljene spojine yttrium je običajno treba posušiti in kazati, da odstranite morebitno preostalo vlago in nečistoče, da končno dobite čisto ytrium kovine ali spojine.
Metode odkrivanja yttrium
Skupne metode odkrivanja za yttrium vključujejo predvsem atomsko absorpcijsko spektroskopijo (AAS), induktivno povezano masno spektrometrijo (ICP-MS), rentgensko fluorescentno spektroskopijo (XRF) itd.
1. Atomska absorpcijska spektroskopija (AAS):AAS je pogosto uporabljena metoda kvantitativne analize, primerna za določanje vsebnosti yttrium v raztopini. Ta metoda temelji na absorpcijskem pojavu, ko ciljni element v vzorcu absorbira svetlobo določene valovne dolžine. Najprej se vzorec pretvori v merljivo obliko s koraki pred obdelavo, kot so zgorevanje plina in visoko temperaturno sušenje. Nato se svetloba, ki ustreza valovni dolžini ciljnega elementa, prenese v vzorec, izmeri intenzivnost svetlobe, ki jo absorbira vzorec, izmerimo in vsebnost ytrija v vzorcu izračunamo tako, da jo primerjamo s standardno raztopino yttrium z znano koncentracijo.
2. Induktivno povezana masna spektrometrija plazme (ICP-MS):ICP-MS je zelo občutljiva analitična tehnika, primerna za določanje vsebnosti yttrium v tekočih in trdnih vzorcih. Ta metoda pretvori vzorec v nabitih delcev in nato za masno analizo uporabi masni spektrometer. ICP-MS ima širok razpon zaznavanja in visoko ločljivost ter lahko hkrati določi vsebino več elementov. Za odkrivanje YTTRIUM-a lahko ICP-MS zagotavlja zelo nizke meje zaznavanja in visoko natančnost.
3. Rentgenska fluorescenčna spektrometrija (XRF):XRF je nedestruktivna analitična metoda, primerna za določanje vsebnosti yttrium v vzorcih trdnih in tekočine. Ta metoda določa vsebnost elementov z obsevanjem površine vzorca z rentgenskimi žarki in merjenjem značilne največje intenzivnosti fluorescenčnega spektra v vzorcu. XRF ima prednosti hitre hitrosti, preprostega delovanja in zmožnosti določanja več elementov hkrati. Vendar pa lahko XRF posežemo pri analizi Yttrium z nizko vsebnostjo, kar ima za posledico velike napake.
4. induktivno povezana spektrometrija optične emisije v plazmi (ICP-OES):Induktivno povezana spektrometrija optične emisije v plazmi je zelo občutljiva in selektivna analitična metoda, ki se široko uporablja pri analizi več elementov. Atomizira vzorec in tvori plazmo za merjenje specifične valovne dolžine in intenzivnosti of yttriumemisija v spektrometru. Poleg zgornjih metod obstajajo tudi druge pogosto uporabljene metode za odkrivanje yttrium, vključno z elektrokemijsko metodo, spektrofotometrijo itd. Izbira primerne metode odkrivanja je odvisna od dejavnikov, kot so lastnosti vzorca, potrebni merilni obseg in natančnost odkrivanja ter standardi kalibracije pogosto potrebni za nadzor kakovosti in zanesljivosti.
Specifična uporaba metode atomske absorpcije yttrium
Pri merjenju elementov je induktivno povezana masna spektrometrija plazme (ICP-MS) zelo občutljiva in več-elementna analiza, ki se pogosto uporablja za določanje koncentracije elementov, vključno z yttrijem. Sledi podroben postopek za testiranje yttrium v ICP-MS:
1. Priprava vzorca:
Vzorec je običajno za analizo ICP-MS običajno raztopiti ali razbiti v tekočo obliko. To je mogoče storiti s kemičnim raztapljanjem, segrevanjem prebave ali drugimi ustreznimi metodami priprave.
Priprava vzorca zahteva izjemno čiste pogoje, da se prepreči kontaminacija s katerim koli zunanjim elementom. Laboratorij bi moral sprejeti potrebne ukrepe, da se prepreči kontaminacija vzorca.
2. Generacija ICP:
ICP nastane z uvedbo mešanega plina argona ali argona-kisika v zaprto kremenčevo plazemsko baklo. Visokofrekvenčna induktivna sklopka daje intenziven plazemski plaz, kar je izhodišče analize.
Temperatura plazme je približno 8000 do 10000 stopinj Celzija, kar je dovolj visoko, da elemente v vzorcu pretvori v ionsko stanje.
3. Ionizacija in ločitev:Ko vzorec vstopi v plazmo, so elementi v njem ionizirani. To pomeni, da atomi izgubijo enega ali več elektronov in tvorijo nabitih ionov. ICP-MS uporablja masni spektrometer za ločevanje ionov različnih elementov, običajno z razmerjem med maso in nabojem (m/z). To omogoča, da se ioni različnih elementov ločijo in nato analizirajo.
4. masna spektrometrija:Ločeni ioni vstopajo v masni spektrometer, običajno kvadrapolen masni spektrometer ali magnetni masni spektrometer za skeniranje. V masnem spektrometru se ioni različnih elementov ločijo in zaznajo glede na njihovo razmerje med maso in nabojem. To omogoča določitev prisotnosti in koncentracije vsakega elementa. Ena od prednosti induktivno povezane plazemske masne spektrometrije je njegova visoka ločljivost, ki mu omogoča, da hkrati zazna več elementov.
5. Obdelava podatkov:Podatke, ki jih ustvari ICP-MS, je treba običajno obdelati in analizirati, da se določi koncentracija elementov v vzorcu. To vključuje primerjavo signala za odkrivanje s standardi znanih koncentracij ter izvajanje kalibracije in korekcije.
6. Rezultat poročila:Končni rezultat je predstavljen kot koncentracija ali masni odstotek elementa. Ti rezultati se lahko uporabijo v različnih aplikacijah, vključno z znanostjo o zemlji, analizo okolja, testiranjem hrane, medicinskimi raziskavami itd.
ICP-MS je zelo natančna in občutljiva tehnika, primerna za analizo več elementov, vključno z yttrium. Vendar pa zahteva zapleteno instrumentacijo in strokovno znanje, zato se običajno izvaja v laboratoriju ali v centru za strokovno analizo. V dejanskem delu je treba izbrati ustrezno metodo merjenja glede na posebne potrebe spletnega mesta. Te metode se pogosto uporabljajo pri analizi in odkrivanju ytterbiuma v laboratorijih in panogah.
Po povzetku zgoraj lahko sklepamo, da je Ytrium zelo zanimiv kemični element z edinstvenimi fizikalnimi in kemičnimi lastnostmi, ki je zelo pomemben na področju znanstvenih raziskav in uporabe. Čeprav smo pri svojem razumevanju tega dosegli nekaj napredka, je še vedno veliko vprašanj, ki potrebujejo nadaljnje raziskave in raziskovanje. Upam, da lahko naš uvod pomaga bralcem bolje razumeti ta očarljiv element in navdihuje ljubezen do znanosti in zanimanja za raziskovanje.
Za več informacij plskontaktirajte nasspodaj:
Tel & kaj: 008613524231522
Email:Sales@shxlchem.com
Čas objave: november-28-2024